Cắt giảm nhiều thủ tục kinh doanh trong lĩnh vực y tế
| Hải quan Gia Thụy: 292 doanh mới về làm thủ tục | |
| Doanh nghiệp Nhật Bản “than” chi phí sản xuất cao, thủ tục còn dài | |
| Ngân hàng “bội thu” từ kinh doanh ngoại hối |
Ngày 12/1 tại Hội nghị Triển khai thông tư số 29/2020/TT-BYT ngày 31/12/2020 của Bộ trưởng Bộ Y tế sửa đổi, bổ sung và bãi bỏ một số văn bản quy phạm pháp luật do Bộ trưởng Bộ Y tế ban hành.
 |
| Nhiều thủ tục hành chính được cắt giảm đã tạo điều kiện cho các DN trong lĩnh vực y tế. |
Theo đó, Thông tư 29 đã sửa đổi một số điều của 11 Thông tư trước đây về quản lý dược phẩm, mỹ phẩm, thực phẩm, HIV theo nguyên tắc tạo điều kiện cho DN trong giai đoạn gặp khó khăn vì đại dịch Covid-19.
Liên quan tới việc cắt giảm thủ tục trong lĩnh vực dược theo ông Chu Quốc Thịnh, Trưởng phòng Quản lý đăng ký thuốc, Cục Quản lý Dược, Thông tư 29 đã bãi bỏ quy định chứng thực chữ ký, tên người ký, dấu cơ quan cấp giấy chứng nhận sản phẩm dược (CPP), giúp Việt Nam có thể hòa nhập quốc tế.
Cụ thể, theo số liệu thống kê hồ sơ đăng ký thuốc nước ngoài đã nộp trong năm 2020, thì dự kiến có khoảng 3.500 hồ sơ đăng ký thuốc nước ngoài mỗi năm được đơn giản hóa thủ tục hành chính.
Còn với hồ sơ thuốc nộp trước ngày 31/12/2021, việc không bắt buộc CPP có đầy đủ các thông tin về tiêu chuẩn thành phẩm, tiêu chuẩn dược chất, nhà sản xuất dược chất dự kiến sẽ giúp đơn giản hóa giấy tờ, tài liệu cho khoảng 7.000 hồ sơ đăng ký thuốc nước ngoài.
Một điểm nữa mà Thông tư 29 có lợi cho DN theo ông Thịnh, nếu trước đây Thông tư 32 quy định thuốc hóa dược mới, sinh phẩm nhập khẩu phải có Giấy chứng nhận sản phẩm dược phẩm (CPP) thứ 2 cấp bởi nước SRA và vắc xin nhập khẩu phải có CPP của nước tham chiếu để đảm bảo chất lượng, an toàn, hiệu quả của thuốc đăng ký lưu hành tại Việt Nam.
Tuy nhiên, qua thực tế cho thấy, nước khác không phải nước sản xuất có thể không cấp CPP cho Việt Nam nếu không trực tiếp xuất khẩu thuốc sang Việt Nam. Việc lưu hành tại nước thứ 2 có thể không phải là CPP, chấp nhận MA hoặc FSC hoặc giấy tờ pháp lý khác.
Do vậy, Thông tư 29 cho phép chấp nhận giấy tờ pháp lý (thứ 2) có nội dung tối thiểu gồm tên thuốc, hoạt chất, nồng độ/hàm lượng hoạt chất, dạng bào chế, tên và địa chỉ cơ sở sản xuất, có xác nhận thuốc được cấp phép và lưu hành thực tế. Đồng thời không yêu cầu giấy tờ pháp lý này nếu sinh phẩm, vắc xin nhập khẩu cấp bởi EMA.
Thông tư 29 quy định việc thay đổi nhỏ chỉ tiêu không cần thông báo (Notification), đã tiết kiệm được tiền lưu kho, bến bãi, nhập cảng cho khoảng 4.200 hồ sơ/năm do được thực hiện ngay mà không cần phải chờ 15 ngày chờ phê duyệt của Cục Quản lý Dược như trước đây.
Đặc biệt, với việc cho phép duy trì hiệu lực số đăng ký 12 tháng cho khoảng 9.000 số đăng ký, sẽ đảm bảo khoảng 9.000 thuốc sẵn sàng cung ứng cho nhu câu điều trị. Điều này bệnh nhân được lợi nhất do không lo thiếu thuốc, không lo khan hiếm nên phải mua giá cao.
Cũng theo ông Thịnh, Thông tư 29 cho phép DN được quyền công bố tá dược, thay cho trước đây tá dược muốn NK về Việt Nam phải có giấy phép NK. Điều này giúp DN cắt giảm thời gian, nhân lực chuẩn bị cho 115.000 hồ sơ cấp phép NK tá dược/năm do không phải làm hồ sơ cấp giầy phép NK.
Về chứng nhận Thực hành tốt sản xuất thuốc (GMP tá dược) - được bãi bỏ cho phép tiết kiệm được số tiền hợp pháp hóa lãnh sự cho DN khoảng 1.4 tỷ đồng/năm (khoảng 9.250 hồ sơ/năm, trong đó, mỗi hồ sơ trung bình 5 tá dược và giá 30.000 VNĐ/bản tài liệu hợp pháp hóa lãnh sự.
Tin liên quan
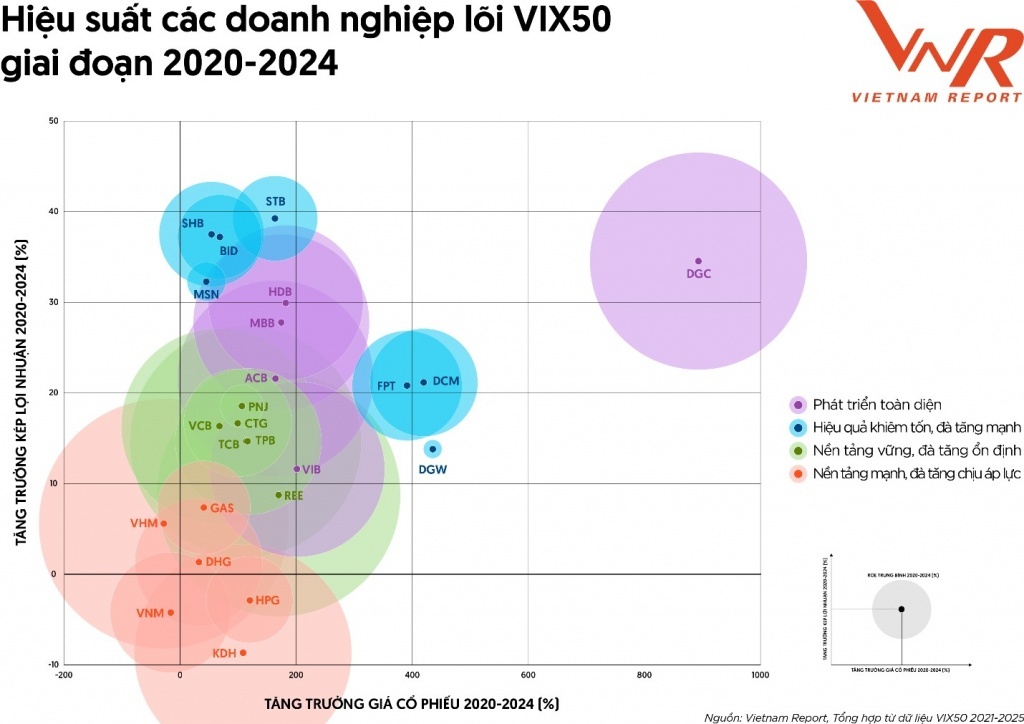
Những doanh nghiệp liên tục góp mặt trong VIX50 suốt 5 năm
08:00 | 05/07/2025 Doanh nghiệp - Thương hiệu

Giảm 50% mức thu của 46 loại phí, lệ phí
21:12 | 03/07/2025 Chính sách thuế, hải quan

Mở rộng diện ưu đãi thuế nhập khẩu để thúc đẩy doanh nghiệp phát triển khoa học công nghệ
09:27 | 03/07/2025 Chính sách thuế, hải quan

Đề xuất hoàn thiện cơ sở pháp lý về thời hạn xử lý nghĩa vụ tài chính đất đai
09:24 | 04/07/2025 Chính sách thuế, hải quan

Hàng hóa phục vụ phát triển khoa học, công nghệ được miễn thuế nhập khẩu
08:31 | 04/07/2025 Chính sách thuế, hải quan

Quy định mới về kiểm tra, xác định trị giá hải quan
08:26 | 04/07/2025 Chính sách thuế, hải quan

Thủ tục xuất nhập khẩu hàng hóa từ kho ngoại quan của doanh nghiệp chế xuất
08:00 | 04/07/2025 Chính sách thuế, hải quan

Thủ tục hải quan khi thay đổi địa chỉ theo đơn vị hành chính mới
20:00 | 03/07/2025 Chính sách thuế, hải quan

Khô dầu hạt cải là mặt hàng nhập khẩu có điều kiện
15:09 | 03/07/2025 Chính sách thuế, hải quan

Quy định giao dịch điện tử đối với hàng XNK và phương tiện XNC, quá cảnh
10:00 | 03/07/2025 Chính sách thuế, hải quan

Những điểm mới cần lưu ý khi triển khai thực hiện quy định về xử lý vi phạm hành chính
07:00 | 03/07/2025 Chính sách thuế, hải quan

Hoá đơn trên 5 triệu đồng phải thanh toán không dùng tiền mặt mới được khấu trừ thuế
16:27 | 02/07/2025 Chính sách thuế, hải quan

Máy móc, thiết bị của DN chế xuất không lưu giữ tại kho thuê ngoài
16:08 | 02/07/2025 Chính sách thuế, hải quan

Hải quan triển khai thực hiện Luật sửa đổi, bổ sung một số điều của Luật Xử lý vi phạm hành chính
15:40 | 02/07/2025 Chính sách thuế, hải quan

Giảm thuế giá trị gia tăng từ 1/7/2025 đến hết 31/12/2026
20:18 | 01/07/2025 Chính sách thuế, hải quan

Người khai hải quan được khai bổ sung thông tin về chứng từ chứng nhận xuất xứ
15:37 | 01/07/2025 Chính sách thuế, hải quan
Vấn đề Bạn quan tâm
Tin mới

Giá Đô la Mỹ trong nước tiếp tục biến động ngược chiều với giá thế giới

Công nghiệp, dịch vụ và tiêu dùng nội địa dẫn dắt tăng trưởng GDP 6 tháng đầu năm 2025

Cảnh sát biển quyết liệt phòng, chống tội phạm, vi phạm pháp luật trên biển

3 kịch bản tác động của thuế đối ứng của Mỹ đối với xuất khẩu Việt Nam

Giá vàng trong nước tháng 6/2025 hạ nhiệt, giảm 1,27% so với tháng 5/2025

(INFORGRAPHICS) - Cơ cấu tổ chức bộ máy mới của ngành Thuế từ ngày 1/7/2025
15:14 | 01/07/2025 Infographics

Bài 3: (LONGFORM): Phân cấp, phân quyền trong quản lý thuế: Tăng hiệu quả, giảm thủ tục vì người dân và doanh nghiệp
15:54 | 30/06/2025 Diễn đàn

(INFOGRAPHICS): Kế hoạch hành động của Cục Thuế để phát triển kinh tế tư nhân
08:59 | 30/06/2025 Infographics

(INFOGRAPHICS): Lưu ý khi làm thủ tục định danh điện tử cho doanh nghiệp, tổ chức
09:00 | 29/06/2025 Infographics

(INFOGRAPHICS): 7 chính sách thuế nổi bật có hiệu lực từ 1/7/2025
09:17 | 27/06/2025 Infographics

Hải quan khu vực XX hướng dẫn doanh nghiệp quy định về ưu đãi đầu tư

Nửa đầu năm, quy mô kim ngạch qua Hải quan khu vực V xấp xỉ 100 tỷ đô

Giải quyết thủ tục hành chính thuế kịp thời đáp ứng yêu cầu chính quyền 2 cấp

Hải quan khu vực XIV: Đảm bảo duy trì hoạt động thông suốt

Công bố lãnh đạo chủ chốt của Thuế tỉnh Phú Thọ

6 tháng đầu năm, Thái Nguyên thu ngân sách đạt 11.062 tỷ đồng

Những doanh nghiệp liên tục góp mặt trong VIX50 suốt 5 năm
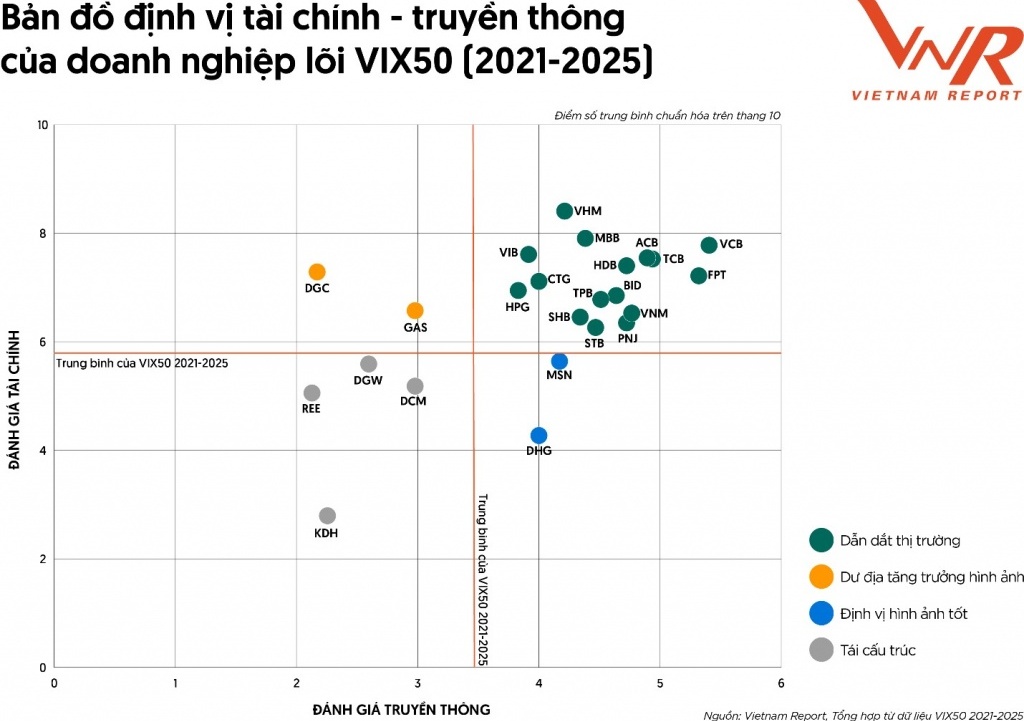
Truyền thông và thương hiệu: Nền móng niềm tin, đòn bẩy giúp doanh nghiệp tăng trưởng

Cỗ máy gia tốc từ Nghị quyết 57-NQ/TW: Một bài học sống động

Hải Phòng sau sáp nhập: Cơ hội mới cho thị trường bất động sản bứt tốc

Cơ hội để ngành điện tử Việt Nam tái cấu trúc

Doveco: Tiên phong sản xuất xanh, khai mở tầm nhìn bền vững cho nông sản Việt

3 kịch bản tác động của thuế đối ứng của Mỹ đối với xuất khẩu Việt Nam

Hoạt động xuất khẩu qua địa bàn Hà Tĩnh tăng trưởng đáng kể

Xuất khẩu rau quả hụt hơi: Chặng nước rút 4,9 tỷ USD khó về đích

Cà phê Việt: Nửa năm, chinh phục trọn kế hoạch

65 tỷ USD: Mục tiêu lớn trên hành trình bền bỉ của nông nghiệp Việt Nam

Chú trọng nâng cao năng lực chế biến sâu và bảo quản nông sản sau thu hoạch

Sàn TMĐT nộp thuế thay, người bán vẫn phải cập nhật thông tin

Hơn 95% hàng hóa Việt Nam hiện diện trong hệ thống phân phối hiện đại

Hậu kiểm thực phẩm online: Sẽ so ảnh mạng, đối chiếu hàng thật

Luật mới sẽ buộc sàn và người bán chia sẻ trách nhiệm

Xăng RON95-III tiếp tục giảm 1.210 đồng/lít, giá tối đa 19.906 đồng/lít

Yêu cầu ngừng kinh doanh, sử dụng 7 sản phẩm dưỡng da của Công ty Toàn Cầu Đông Nam
Lý giải nguyên nhân giá vật liệu xây dựng 6 tháng đầu năm tăng kỷ lục

10/11 nhóm hàng đẩy CPI tháng 6 lên 0,48%

Bất động sản phía Nam đang “hút” dòng tiền đầu tư từ miền Bắc

OCOP Việt: Hành trình vươn ra thế giới

Thị trường bất động sản kỳ vọng sự "bùng nổ"



