Doanh nghiệp thiết bị y tế vướng về chứng chỉ ISO
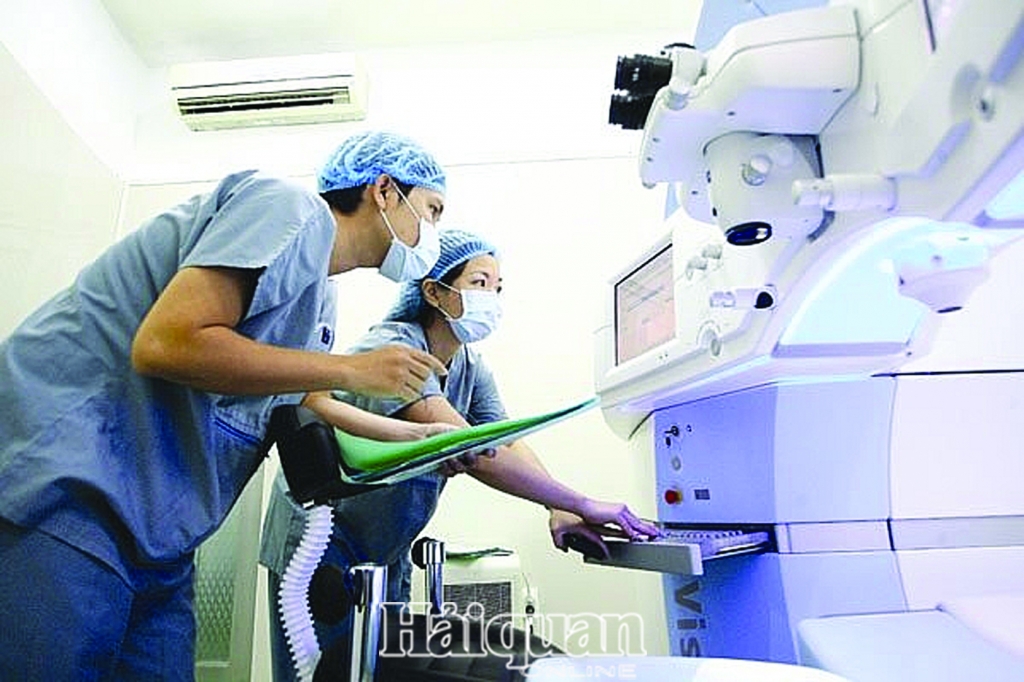 |
| Khung pháp lý về quản lý TTBYT tại Việt Nam đang ngày càng hoàn thiện, song vẫn còn một số bất cập |
Vướng nhiều khâu
Thông tin khái quát nhất về bức tranh hoạt động sản xuất kinh doanh trang thiết bị y tế (TTBYT) của các DN Việt thời gian qua, ông Đoàn Quang Minh, chuyên viên Vụ Trang thiết bị và Công trình y tế cho biết, nếu như năm 2008 nước ta chỉ có 48 DN thì đến nay đã có 318 DN sản xuất TTBYT, với các sản phẩm đa dạng.
Về khó khăn mà các DN sản xuất, kinh doanh TTBYT đang gặp phải, ông Minh cho biết, một số sản phẩm có hàm lượng công nghệ cao như hệ thống chụp X-quang, dao mổ điện, máy theo dõi bệnh nhân... đã được các DN trong nước nghiên cứu, sản xuất thành công nhưng lại gặp khó trong việc tìm thị trường vì khó cạnh tranh với sản phẩm ngoại nhập.
Về phía DN, tại Hội nghị đối thoại với DN về các quy định trong quản lý TTBYT và lấy ý kiến đóng góp về các chính sách hỗ trợ thúc đẩy phát triển sản xuất TTBYT trong nước do Bộ Y tế tổ chức mới đây, bà Phạm Thị Thu Hà, Công ty Siemens Việt Nam cho biết, mặc dù khung pháp lý về quản lý TTBYT tại Việt Nam đang ngày càng hoàn thiện (Chính phủ đã ban hành Nghị định số 36/2016/NĐ-CP và Nghị định số 169/2018/NĐ-CP về quản lý TTBYT, tạo thuận lợi lớn cho các DN trong hoạt động sản xuất, kinh doanh), song, hiện các DN nhập khẩu TTBYT vẫn gặp rất nhiều khó khăn. Đầu tiên là về vấn đề cấp phép đăng ký lưu hành còn chậm do số lượng DN nộp hồ sơ tới Bộ Y tế rất lớn trong khi đó số lượng nhân sự xét duyệt hồ sơ của Bộ Y tế thì ít.
Đại diện Công ty CP Nhựa Y tế Việt Nam (MPV) cho rằng, theo lộ trình sang năm 2020, tất cả DN sản xuất TTBYT đều phải đạt chứng chỉ ISO 13485, tuy nhiên tại Việt Nam, việc cấp chứng chỉ này còn nhiều bất cập, có nhiều tổ chức công nhận không đúng, không được thừa nhận quốc tế. "Hiện Công ty MPV phải ký hợp đồng với các tổ chức nước ngoài để thẩm định nhà máy do vậy mất rất nhiều thời gian, chi phí để thẩm tra và thẩm định. Sau đó phải mất từ 7 đến 9 tháng mới được công nhận ISO 13485”, đại diện Công ty MPV cho biết.
Bộ sẽ gỡ vướng, doanh nghiệp cần "chuẩn chỉ" hơn
Từ những khó khăn mà DN đang gặp phải, đại diện Công ty MPV kiến nghị Bộ Y tế, Bộ Khoa học và Công nghệ siết chặt, kiểm tra các tổ chức công nhận ISO 13485.
Về phía đại diện Công ty TNHH B. Braun Việt Nam kiến nghị các cơ quan quản lý Nhà nước sớm hoàn thiện khung pháp lý về quản lý TTBYT bao gồm các quy định về quản lý chất lượng, sản xuất, đăng ký, quản lý sau bán hàng, nghiên cứu thử nghiệm tiền lâm sàng và lâm sàng. Đồng thời ưu tiên cấp số đăng ký lưu hành cho TTBYT sản xuất trong nước để thúc đẩy sản xuất và xuất khẩu.
Về các đề xuất, kiến nghị của DN nêu trên, ông Nguyễn Minh Tuấn, Vụ trưởng Vụ Trang Thiết bị và Công trình Y tế, Bộ Y tế cho biết, đối với những khó khăn mà DN sản xuất, kinh doanh TTBYT thuộc thẩm quyền của Bộ Y tế, Bộ sẽ xem xét để có điều chỉnh kịp thời. “Song nếu khó khăn mà DN gặp phải thuộc phạm vi của cơ quan khác, Bộ Y tế sẽ có công văn, làm việc chuyên sâu để trao đổi, thảo luận để nhanh chóng tháo gỡ những vướng mắc cho các DN”, ông Nguyễn Minh Tuấn khẳng định.
Tuy nhiên, Vụ trưởng Vụ Trang thiết bị và Công trình y tế cũng cho rằng, bản thân các DN cũng cần lưu ý hơn tới các quy định của cơ quan chức năng để thực hiện cho tốt. Bởi qua quá trình thanh, kiểm tra, cơ quan quản lý nhận thấy nhiều DN kinh doanh TTBYT chưa nghiên cứu kỹ Nghị định số 36, nên nhiều sơ sài, thiếu tài liệu, gửi hồ sơ trực tuyến không đạt yêu cầu; tên TTBYT trên hồ sơ của một số DN bị sai lỗi chính tả, sai tên, không khớp với tên trong bảng phân loại…
"Ngoài ra, các DN kinh doanh TTBYT cũng không hoạt động đúng địa chỉ ghi trong giấy chứng nhận đăng ký kinh doanh, một số có mặt bằng và điều kiện kinh doanh chưa phù hợp với quy mô và hình thức kinh doanh; một số đơn vị được Bộ Y tế công bố đủ điều kiện phân loại TTBYT nhưng phân loại sai cho các DN sản xuất, kinh doanh hoặc một số DN tự phân loại TTBYT khi chưa đủ điều kiện, chưa được Bộ Y tế cấp phép", ông Tuấn nêu.
Tin liên quan
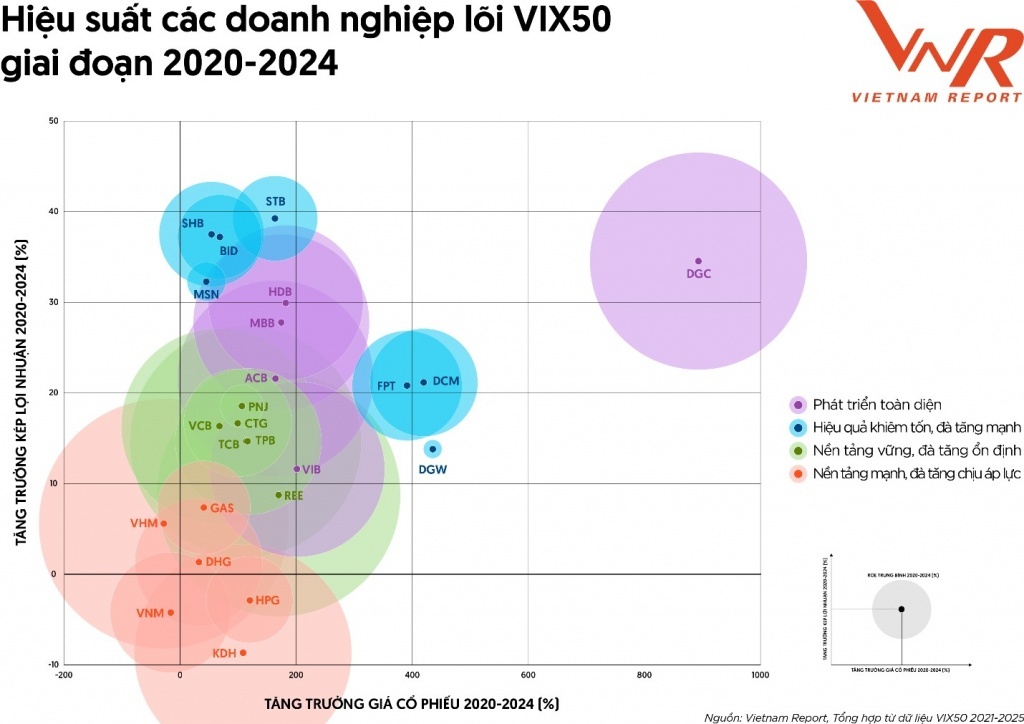
Những doanh nghiệp liên tục góp mặt trong VIX50 suốt 5 năm
08:00 | 05/07/2025 Doanh nghiệp - Thương hiệu

Giảm 50% mức thu của 46 loại phí, lệ phí
21:12 | 03/07/2025 Chính sách thuế, hải quan

Mở rộng diện ưu đãi thuế nhập khẩu để thúc đẩy doanh nghiệp phát triển khoa học công nghệ
09:27 | 03/07/2025 Chính sách thuế, hải quan

Viettel "bắt tay" OPPO: Thúc đẩy phổ cập 5G và trải nghiệm AI tại Việt Nam
15:28 | 04/07/2025 Thị trường - Doanh nghiệp

Vietjet mở lối khám phá thung lũng Swan: Thiên đường cho kẻ mộng mơ và tín đồ ẩm thực
16:28 | 30/06/2025 Thị trường - Doanh nghiệp

Không có sự khác biệt nào giữa một tỷ phú với một bác tài Tuk tuk trong thế giới AI
14:19 | 26/06/2025 Thị trường - Doanh nghiệp

Binh đoàn 20 bàn giao công trình sửa chữa nhà đồng đội
17:26 | 25/06/2025 Thị trường - Doanh nghiệp
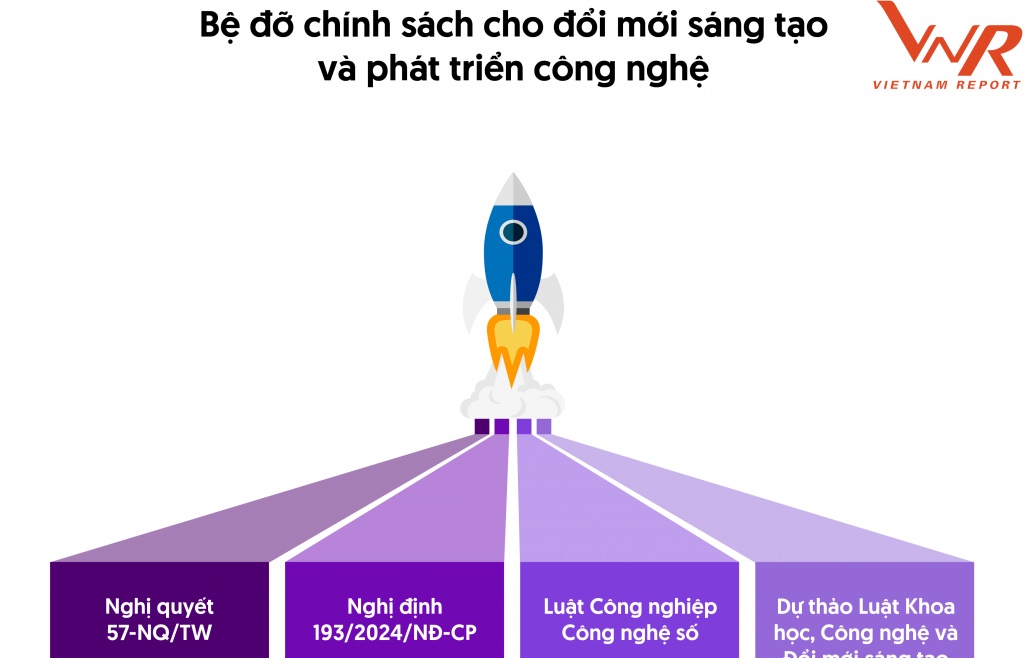
Top 10 công ty công nghệ uy tín năm 2025 sẵn sàng “vươn mình” cùng “bệ phóng” chính sách
16:32 | 22/06/2025 Thị trường - Doanh nghiệp

“Mở khóa” dinh dưỡng tự nhiên bằng công nghệ: Sữa Việt tạo tiếng vang tại sân chơi toàn cầu
10:28 | 21/06/2025 Thị trường - Doanh nghiệp

Vietjet đồng hành cùng người hâm mộ đến K-Star Spark 2025 tại Hà Nội
20:46 | 20/06/2025 Thị trường - Doanh nghiệp
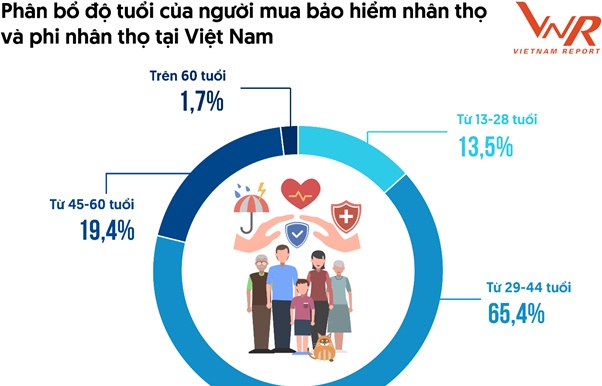
Từ số hóa đến cá nhân hóa: Gen Y và Gen Z đang tái định hình thị trường bảo hiểm Việt Nam
20:47 | 13/06/2025 Thị trường - Doanh nghiệp

HDBank hợp tác BIDV triển khai nguồn vốn quốc tế thúc đẩy phát triển bền vững
11:20 | 13/06/2025 Thị trường - Doanh nghiệp
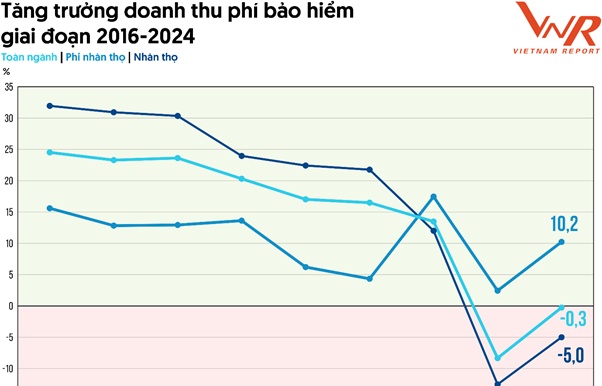
Thị trường bảo hiểm Việt Nam 2025: Tái thiết niềm tin, hướng tới phát triển bền vững
18:33 | 12/06/2025 Thị trường - Doanh nghiệp

Cần cơ chế “mở khóa” để nhà ở xã hội không bị đẩy lên cao
18:15 | 12/06/2025 Thị trường - Doanh nghiệp

Nhiều dự án khởi nghiệp xanh đã có sản phẩm xuất khẩu
14:29 | 12/06/2025 Thị trường - Doanh nghiệp

Ngành ngân hàng dẫn đầu phát hành trái phiếu doanh nghiệp
10:16 | 11/06/2025 Doanh nghiệp - Thương hiệu
Vấn đề Bạn quan tâm
Tin mới

Giá Đô la Mỹ trong nước tiếp tục biến động ngược chiều với giá thế giới

Công nghiệp, dịch vụ và tiêu dùng nội địa dẫn dắt tăng trưởng GDP 6 tháng đầu năm 2025

Cảnh sát biển quyết liệt phòng, chống tội phạm, vi phạm pháp luật trên biển

3 kịch bản tác động của thuế đối ứng của Mỹ đối với xuất khẩu Việt Nam

Giá vàng trong nước tháng 6/2025 hạ nhiệt, giảm 1,27% so với tháng 5/2025

(INFORGRAPHICS) - Cơ cấu tổ chức bộ máy mới của ngành Thuế từ ngày 1/7/2025
15:14 | 01/07/2025 Infographics

Bài 3: (LONGFORM): Phân cấp, phân quyền trong quản lý thuế: Tăng hiệu quả, giảm thủ tục vì người dân và doanh nghiệp
15:54 | 30/06/2025 Diễn đàn

(INFOGRAPHICS): Kế hoạch hành động của Cục Thuế để phát triển kinh tế tư nhân
08:59 | 30/06/2025 Infographics

(INFOGRAPHICS): Lưu ý khi làm thủ tục định danh điện tử cho doanh nghiệp, tổ chức
09:00 | 29/06/2025 Infographics

(INFOGRAPHICS): 7 chính sách thuế nổi bật có hiệu lực từ 1/7/2025
09:17 | 27/06/2025 Infographics

Hải quan khu vực XX hướng dẫn doanh nghiệp quy định về ưu đãi đầu tư

Nửa đầu năm, quy mô kim ngạch qua Hải quan khu vực V xấp xỉ 100 tỷ đô

Giải quyết thủ tục hành chính thuế kịp thời đáp ứng yêu cầu chính quyền 2 cấp

Hải quan khu vực XIV: Đảm bảo duy trì hoạt động thông suốt

Công bố lãnh đạo chủ chốt của Thuế tỉnh Phú Thọ

6 tháng đầu năm, Thái Nguyên thu ngân sách đạt 11.062 tỷ đồng

Những doanh nghiệp liên tục góp mặt trong VIX50 suốt 5 năm
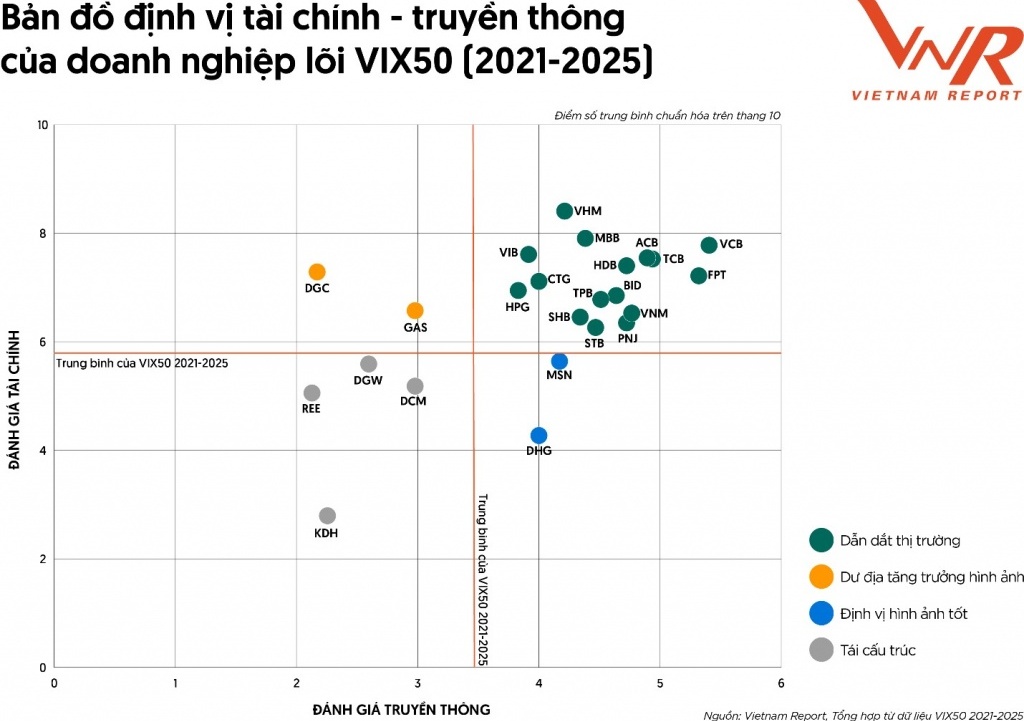
Truyền thông và thương hiệu: Nền móng niềm tin, đòn bẩy giúp doanh nghiệp tăng trưởng

Cỗ máy gia tốc từ Nghị quyết 57-NQ/TW: Một bài học sống động

Hải Phòng sau sáp nhập: Cơ hội mới cho thị trường bất động sản bứt tốc

Cơ hội để ngành điện tử Việt Nam tái cấu trúc

Doveco: Tiên phong sản xuất xanh, khai mở tầm nhìn bền vững cho nông sản Việt

Đề xuất hoàn thiện cơ sở pháp lý về thời hạn xử lý nghĩa vụ tài chính đất đai

Hàng hóa phục vụ phát triển khoa học, công nghệ được miễn thuế nhập khẩu

Quy định mới về kiểm tra, xác định trị giá hải quan

Thủ tục xuất nhập khẩu hàng hóa từ kho ngoại quan của doanh nghiệp chế xuất

Giảm 50% mức thu của 46 loại phí, lệ phí

Thủ tục hải quan khi thay đổi địa chỉ theo đơn vị hành chính mới

3 kịch bản tác động của thuế đối ứng của Mỹ đối với xuất khẩu Việt Nam

Hoạt động xuất khẩu qua địa bàn Hà Tĩnh tăng trưởng đáng kể

Xuất khẩu rau quả hụt hơi: Chặng nước rút 4,9 tỷ USD khó về đích

Cà phê Việt: Nửa năm, chinh phục trọn kế hoạch

65 tỷ USD: Mục tiêu lớn trên hành trình bền bỉ của nông nghiệp Việt Nam

Chú trọng nâng cao năng lực chế biến sâu và bảo quản nông sản sau thu hoạch
Lý giải nguyên nhân giá vật liệu xây dựng 6 tháng đầu năm tăng kỷ lục

10/11 nhóm hàng đẩy CPI tháng 6 lên 0,48%

Bất động sản phía Nam đang “hút” dòng tiền đầu tư từ miền Bắc

OCOP Việt: Hành trình vươn ra thế giới

Thị trường bất động sản kỳ vọng sự "bùng nổ"




